Allergen-Immuntherapie (AIT)
Allgemeine Informationen
Die Allergen-Immuntherapie, auch als „Hyposensibilisierung“ oder „spezifische Immuntherapie“ bezeichnet, ist indiziert bei IgE-vermittelten Allergien, die sich als Rhinokonjunktivitis oder Asthma äußern.
Das Ziel der AIT ist es, die Intensität der Symptome, die bei einem sensibilisierten Patienten bei einer Allergenexposition auftreten, soweit wie möglich zu reduzieren. Der Patient wird infolge der Verabreichung steigender Dosen der verantwortlichen Allergene gegenüber diesen Allergenen tolerant.
Neben der Allergenkarenz ist die AIT von der WHO als einzige Behandlungsform anerkannt, die den
natürlichen Verlauf der allergischen Erkrankung beeinflussen kann.1
Die Indikationen und Kontraindikationen der Allergenimmuntherapie sowie die Modalitäten für ihre Durchführung und Kontrolle sind in einem internationalen Konsensuspapier festgelegt. Das 2001 verfasste ARIA-Konsensuspapier (Allergic Rhinitis and its Impact on Asthma) gibt der Allergenimmuntherapie einen eindeutigen Platz bei der Behandlung der allergischen Rhinitis.1
Die Allergenimmuntherapie wirkt vor allem dem allergischen Entzündungsprozess entgegen, da sie die Entwicklung einer Rhinitis zu Asthma verhindert. Ihre günstige Wirkung hält zudem lange nach Ende der Behandlung an.1
Wirkmechanismus
Bei der Allergenimmuntherapie werden über einen längeren Zeitraum regelmäßig Allergene appliziert. Dadurch kommt es zu einer Modulation der T-Zell- und B-Zell-Antworten bei Allergenexposition und einer damit verbundenen Veränderung der Freisetzung von Antikörper-Subtypen. Auch die Reaktivität von Effektorzellen wie Eosinophilen, Basophilen und Mastzellen wird reduziert2–5. Das klinische Resultat ist eine Abnahme der allergischen Symptome.
Nach heutigem Wissensstand2,3,6–10 geht man davon aus, dass die immunologischen Mechanismen der Allergenimmuntherapie wie folgt ablaufen:
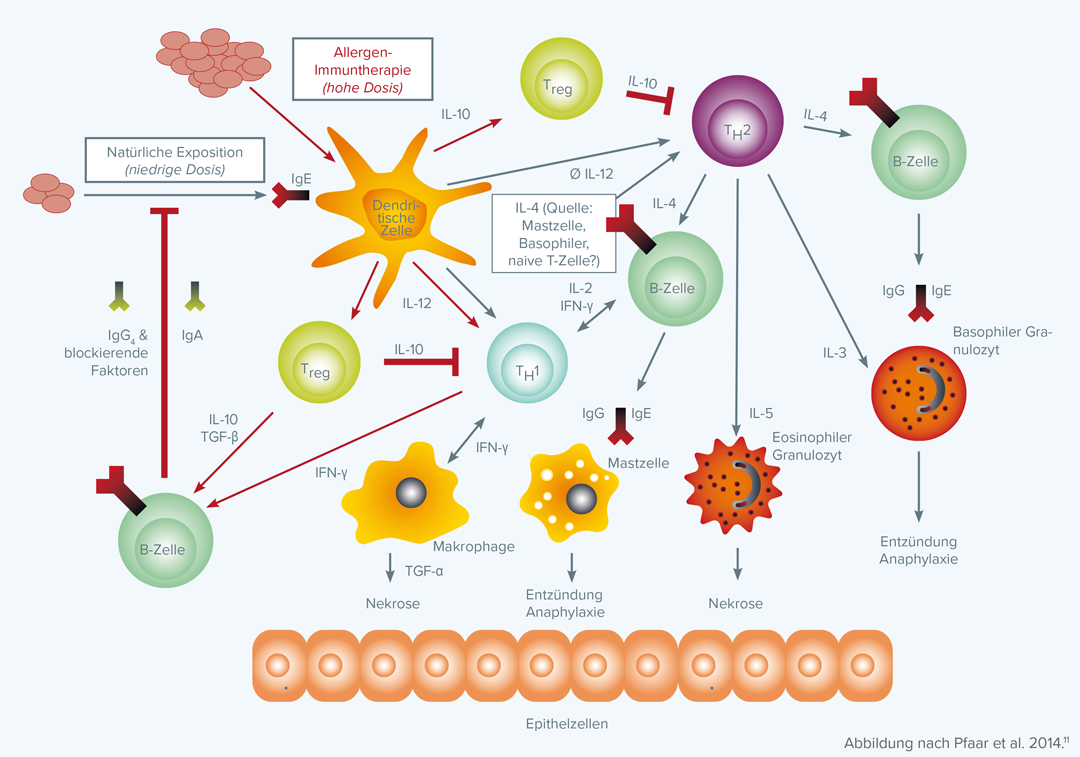
- Aktivierung von Antikörpern, die die allergenantikörpervermittelte Immunantwort blocken. Die aktivierten Antikörper sind vor allem IgG- und IgA-Antikörper, die in der Lage sind, die Bindung von IgE-Allergen-Komplexen an B-Zellen und dendritische Zellen zu verhindern. Dies trägt entscheidend zum Behandlungserfolg der AIT bei.
- Aktivierung von regulatorischen T-Zellen (Tregs), die in der Lage sind, die T-Zellvermittelte Aktivierung von B-Zellen zu unterdrücken und gleichzeitig die allergenspezifische T-Zell- Antwort zu unterbinden. Die Tregs setzen die anti-inflammatorischen Zytokine IL-10 und TGF-ß am Ort der Entzündungsreaktion frei, wodurch die Entzündung abgeschwächt wird. Auch die Bildung regulatorischer B-Zellen ist mittlerweile belegt.17
- Neben den Tregs sind auch die lokalen dendritischen Zellen in der Lage, IL-10 und TGF-ß freizusetzen, als Reaktion auf ihre Aktivierung durch das Allergen. So wird die Entzündungsreaktion weiter abgeschwächt. IL-10 stimuliert darüber hinaus B-Zellen zur weiteren IgG-Produktion, was den unter Punkt 1 genannten Effekt verstärkt.
- Durch die Freisetzung weiterer Zytokine und die damit einhergehende Abschwächung der Mastzellaktivität, sowie die Inhibierung weiterer Entzündungsmediatoren, wird die allergische Entzündungsreaktion weiter abgeschwächt.
Spezielle Aspekte bei der SLIT (Sublinguale Immuntherapie)
Ein entscheidendes Merkmal der SLIT ist die orale Aufnahme des Allergens über die Mundschleimhaut. Die sublinguale Verabreichung von Allergentabletten oder -lösungen und deren Halten unter der Zunge für einige Minuten vor dem Schlucken konzentriert das Allergen weitestgehend auf das sublinguale Gewebe.
Nach der Aufnahme befindet sich das Allergen über mehrere Stunden in der sublingualen Schleimhaut und führt zu einer frühzeitigen Erhöhung des antigenspezifischen IgE.
Immuntoleranz durch die SLIT entsteht durch die oralen Langerhanszellen, die die Induktion von CD4+-regulatorischen T-Zellen und die Produktion von allergenspezifischen blockierenden antiinflammatorischen IgG- und IgA-Antikörpern antreiben.12,13
Die Mundhöhle ist eine natürlich tolerogene Umgebung, die sich trotz kontinuierlicher Exposition gegenüber multiplen Fremdproteinen bei einem gesunden Menschen nicht entzündet.
Das Vorhandensein von Langerhanszellen und Monozyten, die in der Lage sind, IL-10 und TGF-β zu produzieren, tragen wesentlich zur Erhaltung der Toleranz bei.14 T-Zellen aus der menschlichen Mundschleimhaut produzieren TGF-β1, IL-10, Interferon-γ und IL-17, und, insbesondere in der Vestibularregion, toll-like receptor (TLR) 2 und TLR4. Orale Langerhanszellen sind in der Lage, Allergene wie z.B. Phl p 5 schnell (innerhalb von 5 Minuten) aufzunehmen, was zu einer Abschwächung ihrer Reifung und zu einer erhöhten Produktion von anti-inflammatorischen Zytokinen (IL-10 und TGF-β) führt.15
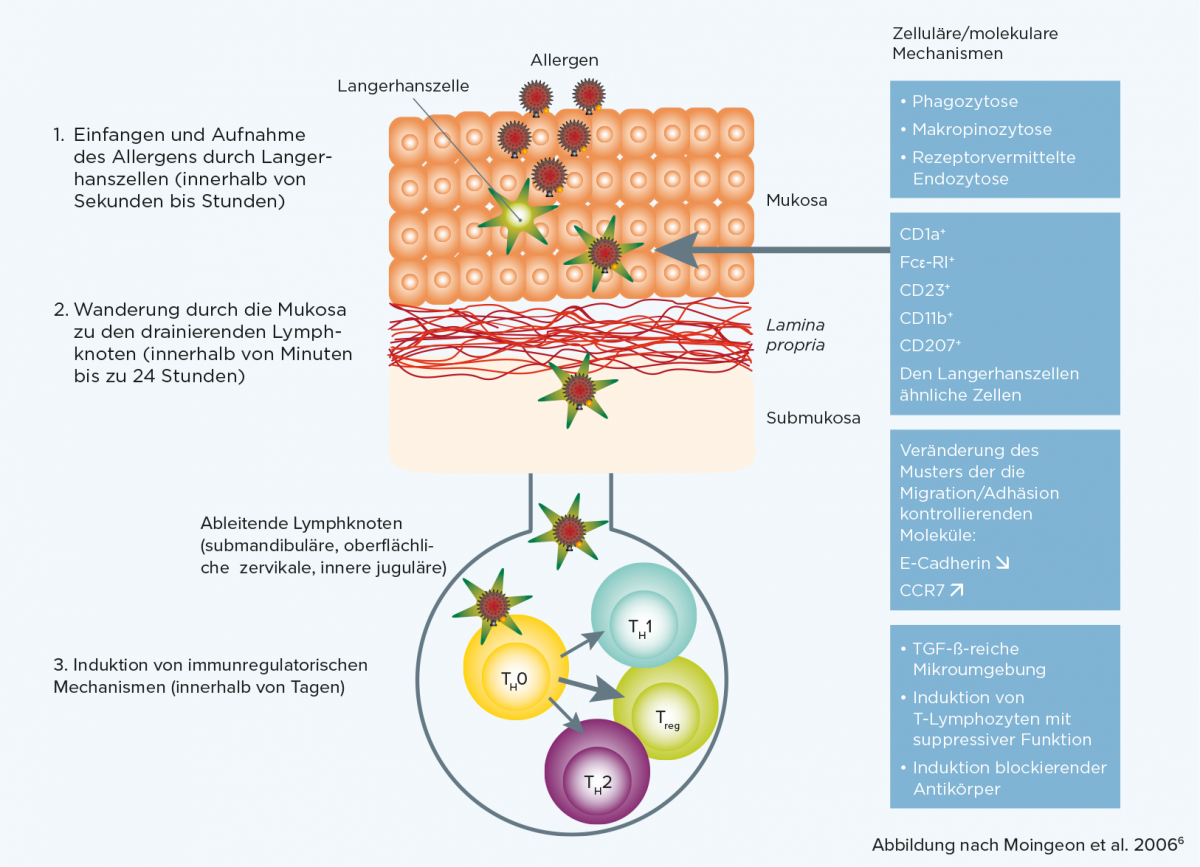
Um eine therapeutisch ausreichende Aufnahme der Allergene bei der sublingualen Allergenimmuntherapie zu erreichen, wird die Allergenlösung oder die Allergentablette für einige Zeit (etwa 1 bis 2 Minuten) unter der Zunge gehalten. Dadurch wird eine Intensivierung des Allergenkontakts mit der Mundschleimhaut erreicht, um so optimale Bedingungen für die Bindung des Allergens durch die oralen Langerhanszellen zu schaffen.
Nach Aufnahme des Allergens durch die oralen Langerhanszellen wandern die Allergene zu den drainierenden Lymphknoten, präsentieren dort die während der Wanderung prozessierten Peptidfragmente mit den allergenspezifischen T-Zell-Epitopen und induzieren über den T-Zell-Kontakt immunregulatorische Mechanismen. Die Allergenaufnahme ist dabei dosisabhängig.7
Wirksamkeit
Die Allergenimmuntherapie ist die einzige Behandlungsform, die den natürlichen Verlauf allergischer Erkrankungen beeinflussen kann.16 Die Wirksamkeit der AIT bei allergischer Rhinitis und allergischem Asthma konnte in zahlreichen placebokontrollierten Doppelblindstudien nachgewiesen werden. Ihre Wirksamkeit zeigt sich durch:
Reduktion des Medikamentenverbrauchs (symptomatisch wirksame Bedarfsmedikation)
Verbesserung der allergischen Symptome

